BRASIL
Petrobras aumenta preços da gasolina e do diesel nas refinarias
segunda-feira, 8 de março de 2021
Segura o bolso. A Petrobras anunciou nesta segunda-feira 8/3, um novo aumento dos preços da gasolina e do diesel que são cobrados em suas refinarias. No caso da gasolina, o aumento é o sexto do ano, e o preço médio do litro passará de R$ 2,60 para R$ 2,84, em uma alta de cerca de 9,2%.
Para o litro do diesel, o reajuste anunciado é de R$ 2,71 para R$ 2,86, um encarecimento de cerca de 5,5%. No caso desse combustível, o aumento é o quinto no ano.
O último reajuste havia sido anunciado pela Petrobras em 1° de março e, antes disso, houve aumentos em 18 de fevereiro, 8 de fevereiro, 26 de janeiro e 18 de janeiro, dia em que apenas o preço da gasolina foi reajustado. No fim do ano passado, o litro de combustível custava R$ 1,84 nas refinarias, R$ 1 a menos que o preço alcançado hoje.
Política de preços
A política de preços da Petrobras busca o alinhamento do preço das refinarias aos do mercado internacional, o que também torna o preço sensível ao valor do real perante o dólar, moeda em que as negociações ocorrem no exterior.
Segundo a estatal, manter esse alinhamento é fundamental para garantir que o mercado brasileiro seja suprido sem risco de desabastecimento. A empresa afirma que, assim como o preço sobe quando há encarecimento no mercado internacional, ele também cai quando a alta da oferta no mundo desvaloriza esses combustíveis.
A Petrobras destaca ainda que essas variações do mercado internacional e do câmbio “têm influência limitada” no preço final que os consumidores encontram nos postos de combustíveis. “Até chegar ao consumidor são acrescidos tributos federais e estaduais, custos para aquisição e mistura obrigatória de biocombustíveis, além das margens brutas das companhias distribuidoras e dos postos revendedores de combustíveis”.
Fotografia/Fonte: Agência Brasil
Ministro informa o valor médio do auxílio emergencial
segunda-feira, 8 de março de 2021
O ministro da Economia, Paulo Guedes, disse nesta segunda-feira 8/3, que o valor médio do novo auxílio emergencial deve ser de R$ 250 por pessoa. A declaração foi dada em entrevista à imprensa no Palácio do Planalto, após reunião com o presidente Jair Bolsonaro para tratar da compra da vacinas contra covid-19. “É vacina, e justamente manter a economia em movimento, esta é a prioridade do governo”, disse.
A expectativa é que o valor comece a ser pago ainda neste mês, com a aprovação da Proposta de Emenda à Constituição 186/2019, a chamada PEC Emergencial. O texto possibilita o pagamento do auxílio com créditos extraordinários sem ferir o teto de gastos públicos.
De acordo com Guedes, a decisão sobre a amplitude do auxílio emergencial é do Ministério da Cidadania. “Nós [Ministério da Economia] só fornecemos os parâmetros básicos”, disse o ministro. Segundo ele, o valor para mulher chefe de família monoparental deve ser de R$ 375 e, no caso de homem, de R$ 175. “Se for casal, já são R$ 250”, informou.
O auxílio emergencial foi criado em abril do ano passado pelo governo federal para atender pessoas vulneráveis afetadas pela pandemia de covid-19. Ele foi pago em cinco parcelas de R$ 600 ou R$ 1,2 mil para mães chefes de família monoparental e, depois, estendido até 31 de dezembro em até quatro parcelas de R$ 300 ou R$ 600 cada.
Tiveram direito aos repasses, obedecendo a uma série de critérios econômicos e sociais, integrantes do Bolsa Família, cidadãos incluídos no Cadastro Único (CadÚnico), além de trabalhadores informais, contribuintes individuais do Instituto Nacional do Seguro Social (INSS) e microempreendedores individuais que solicitaram o benefício por meio de plataformas digitais ou aplicativo da Caixa Econômica Federal.
Fotografia/Fonte: Agência Brasil
Ministro do STF anula condenações de Lula na Lava Jato
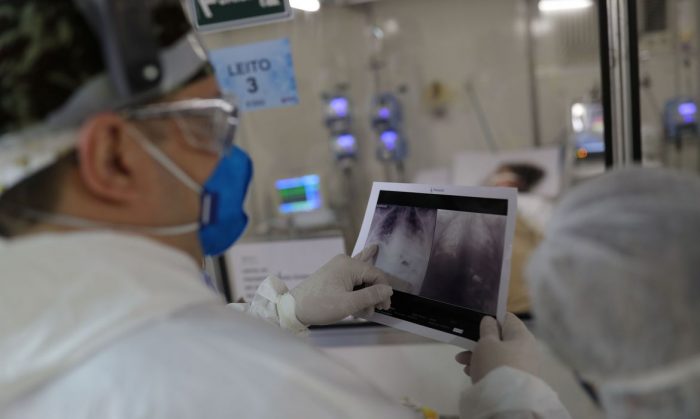
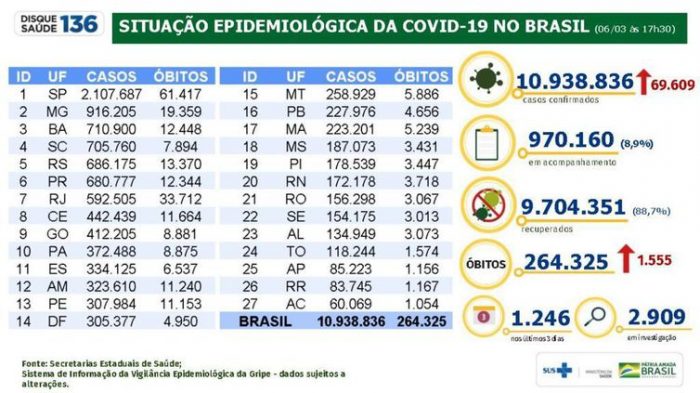
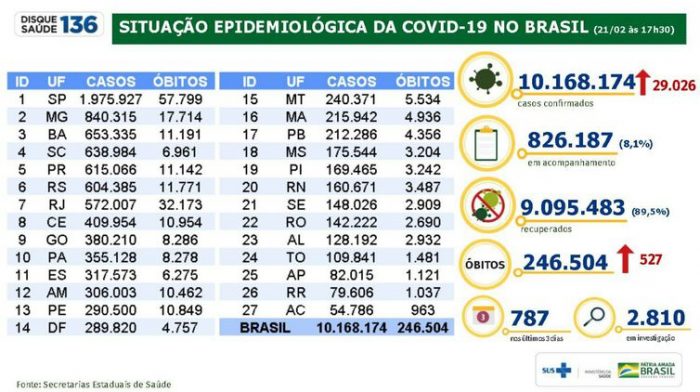
segunda-feira, 8 de março de 2021Covid-19: mortes ultrapassam 264 mil e casos chegam a quase 11 milhões
domingo, 7 de março de 2021Covid-19: Empresa confirma 13 milhões de doses da vacina para o Brasil
sábado, 6 de março de 2021Senado aprova em segundo turno PEC Emergencial
quinta-feira, 4 de março de 2021PF deflagra nova operação contra fraudes no auxílio emergencial
quinta-feira, 4 de março de 2021Brasil registra maior número de mortes em 24h durante toda a pandemia
quarta-feira, 3 de março de 2021Anvisa diz que vacinas usadas no Brasil são seguras
quarta-feira, 3 de março de 2021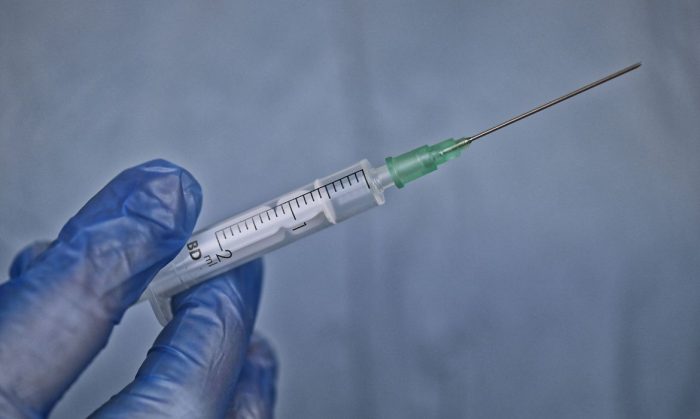
Olha aí. A Agência Nacional de Vigilância Sanitária (Anvisa) informou que, até o momento, os dados públicos de notificações do uso de vacinas contra covid-19 no país não indicam qualquer relação das vacinas com eventos adversos graves ou mortes. De acordo com a Anvisa, não houve alteração na relação de risco e benefício dos produtos.
Em nota, a agência reguladora explicou que a avaliação benefício-risco leva em conta um conjunto grande de informações e os registros informados pelos usuários são apenas uma dessas fontes. As outras envolvem os relatórios de segurança das fabricantes, os sinais de segurança gerados pelo modelo matemático da Organização Mundial da Saúde (OMS), a troca de informações com outras autoridades regulatórias e a discussão em grupos de especialistas.
“Até o momento, não há nenhum caso de óbito conhecido que tenha relação estabelecida com o uso das vacinas para covid-19 autorizadas no país. As vacinas em uso no Brasil são consideradas seguras”, informou a agência. “Já é esperado que pessoas venham a óbito por outros motivos de saúde e mesmo por causas naturais, tendo em vista a taxa de mortalidade já conhecida para cada faixa etária da população brasileira”, completou.
As notificações sobre vacinas e medicamentos são enviadas à Anvisa principalmente por profissionais e serviços de saúde, além dos próprios fabricantes que são obrigados a comunicar os eventos suspeitos e que possam ser graves. Esses dados são utilizados pela Anvisa como subsídio para o seu processo de monitoramento.
“Como são dados notificados por terceiros, eles são considerados de menor evidência científica e servem apenas como sinalizadores para o trabalho de monitoramento da Anvisa. A análise completa envolve os processos mencionados anteriormente”, explicou.
Atualmente, estão autorizadas para uso emergencial no Brasil a vacina Covishield, desenvolvida pela Universidade de Oxford em parceria com a farmacêutica britânica AstraZeneca, e produzida no país pela Fundação Oswaldo Cruz (Fiocruz); e a vacina CoronaVac, produzida pelo Instituto Butantan em parceria com a farmacêutica chinesa Sinovac. Elas estão sendo adquiridas e distribuídas pelo Ministério da Saúde aos estados para vacinação da população dentro do Programa Nacional de Imunizações (PNI).
A Anvisa também concedeu registro para a vacina Cominarty, desenvolvida pela farmacêutica norte-americana Pfizer em parceria com a empresa de biotecnologia alemã BioNtech. Nesse caso, o registro é definitivo, para uso amplo, entretanto, o imunizante ainda não está disponível no país.
Fonte: Agência Brasil
Fotografia: Reprodução
Homem é morto por sete cães da raça pitbull
quarta-feira, 3 de março de 2021Câmara aprova projeto para compra de vacinas por estados
quarta-feira, 3 de março de 2021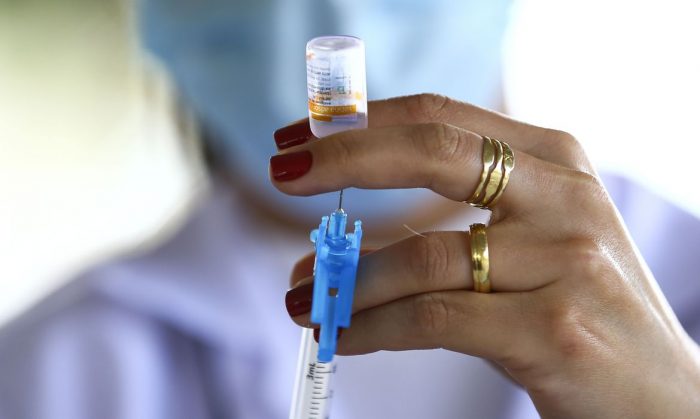
A Câmara dos Deputados aprovou na terça-feira 2/3, o projeto de lei que autoriza os estados, os municípios e o setor privado a comprar vacinas contra a covid-19 com registro ou autorização temporária de uso no Brasil. No caso do setor privado, as doses devem ser integralmente doadas ao Sistema Público de Saúde (SUS) enquanto o público prioritário não tiver sido todo vacinado. A matéria segue para sanção presidencial.
O texto é de autoria do presidente do Senado, Rodrigo Pacheco (DEM-MG). A matéria foi aprovada pelos senadores em fevereiro. O parecer do deputado Igor Timo (Pode-MG) propôs aprovação do texto sem mudanças.
“Em se tratando da vacina, não há nenhuma possibilidade de furar fila, haja vista que serão feitas doações em 100% para que os grupos de risco sejam vacinados prioritariamente e, em um segundo momento, 50% de toda a vacina que for adquirida, seguindo os critérios do Plano Nacional de Imunização”, afirmou Timo.
Fotografia/Fonte: Agência Brasil
“Dia inesquecível”, diz Pelé ao ser vacinado contra covid-19
terça-feira, 2 de março de 2021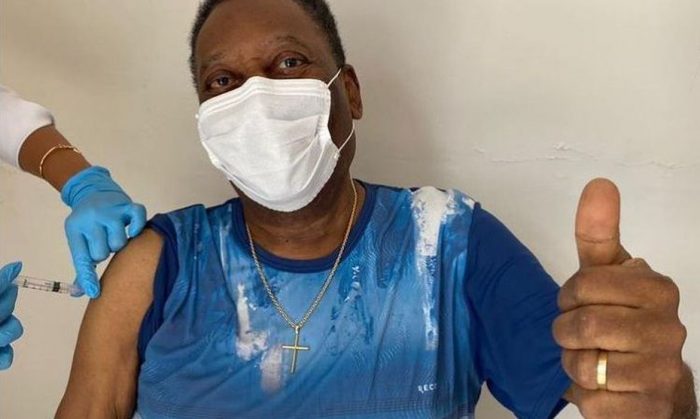
O tricampeão mundial Pelé, de 80 anos, foi vacinado nesta terça-feira contra a Covid-19 e comemorou o “dia inesquecível”, mas alertou que a pandemia ainda não acabou e que as pessoas devem cumprir as medidas de prevenção para evitar mais mortes.
Uma foto do momento em que o ex-jogador recebeu a primeira dose do imunizante tirada por sua esposa Marcia Aoki foi publicada nas redes sociais de Pelé. Na imagem, ele faz sinal de positivo ao receber a injeção.
“Hoje foi um dia inesquecível. Eu recebi a vacina!”, disse Pelé em texto que acompanha a publicação. “A pandemia ainda não acabou. Nós precisamos manter a disciplina para preservar vidas enquanto muitas pessoas ainda não foram imunizadas. Por favor, lavem bem as mãos e continuem em casa, se possível. Quando você sair, não esqueça de usar máscara e de manter o distanciamento social. Isso vai passar se conseguirmos pensar no próximo e ajudar uns aos outros”, acrescentou.
Pelé, que completou 80 anos em outubro, recebeu a vacina por fazer parte do grupo prioritário devido à idade. Ele passa a maior parte do tempo em casa no Guarujá (SP) para se proteger da pandemia.
Atualmente Pelé caminha com dificuldades devido a um problema no quadril. Nos últimos anos ele passou por hospitalizações por diferentes problemas de saúde.
Fotografia/Fonte: Agência Brasil
Caixa com mais de 10 serpentes é encontrada em agência dos Correios
terça-feira, 2 de março de 2021Técnicos da Anvisa inspecionam laboratório indiano que produz Covaxin
segunda-feira, 1 de março de 2021
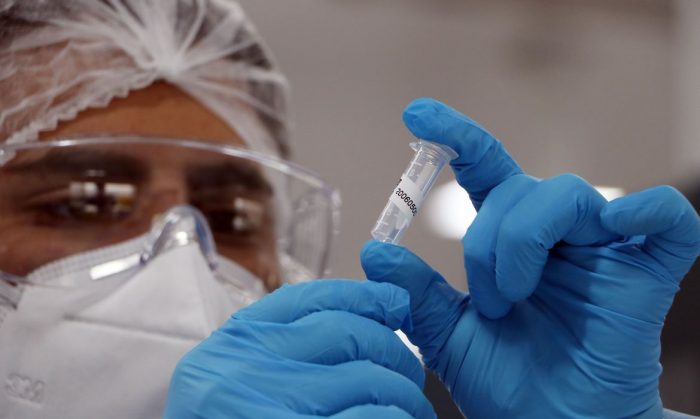
Olha aí. Técnicos da Agência Nacional de Vigilância Sanitária (Anvisa) visitaram nesta segunda-feira, dia 1º/3, a fábrica da empresa Bharat Biotech, na Índia. Realizada a pedido da própria companhia, a inspeção às instalações onde está sendo produzida a vacina Covaxin, contra a covid-19, está prevista para terminar na sexta-feira, dia 5/3.
Cinco servidores da agência reguladora brasileira avaliarão os padrões de produção da matéria-prima usada na elaboração do imunizante e da própria vacina. Os técnicos vão analisar os procedimentos de armazenamento, os processos de trabalho, entre outros critérios de controle de qualidade, cuja observância é necessária para que a Anvisa conceda ao laboratório farmacêutico o Certificado de Boas Práticas de Fabricação – documento que a agência emite aos fabricantes de medicamentos, produtos para a saúde, cosméticos, perfumes, produtos de higiene pessoal, saneantes e insumos farmacêuticos do Brasil e de outros países que cumprem os procedimentos e práticas estabelecidos pela instituição.
A Bharat Biotech ainda não pediu à Anvisa autorização para realização de estudos clínicos da Covaxin no Brasil, nem o registro de uso emergencial da vacina no país. Apesar disso, na quinta-feira, dia 25/3, o Ministério da Saúde assinou um contrato para comprar 20 milhões de doses do imunizante produzido pelo laboratório.
O contrato assinado com a Precisa Medicamentos, responsável por importar a Covaxin no Brasil, está orçado em R$ 1,614 bilhão. E prevê a entrega dos medicamentos de maneira escalonada, entre os meses de março (quando o país receberia os primeiros 8 milhões de doses) e maio deste ano.
Fonte: Agência Brasil
Fotografia: Reprodução
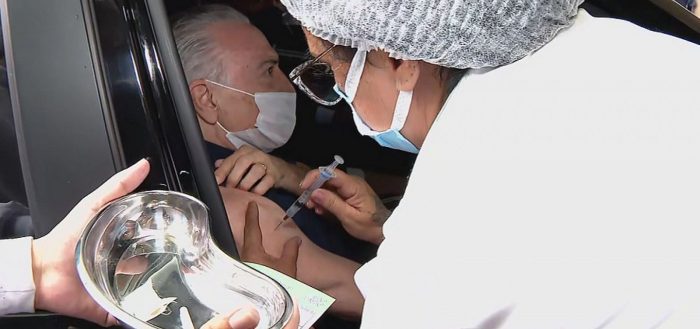
Ex-presidente Michel Temer é vacinado contra a Covid-19
domingo, 28 de fevereiro de 2021Presidente da República fala sobre a volta do auxílio emergencial
sexta-feira, 26 de fevereiro de 2021Covid-19: Brasil registrou mais de 60 mil infectados em 24 horas
quarta-feira, 24 de fevereiro de 2021Anvisa aprova registro definitivo para a vacina da Pfizer
terça-feira, 23 de fevereiro de 2021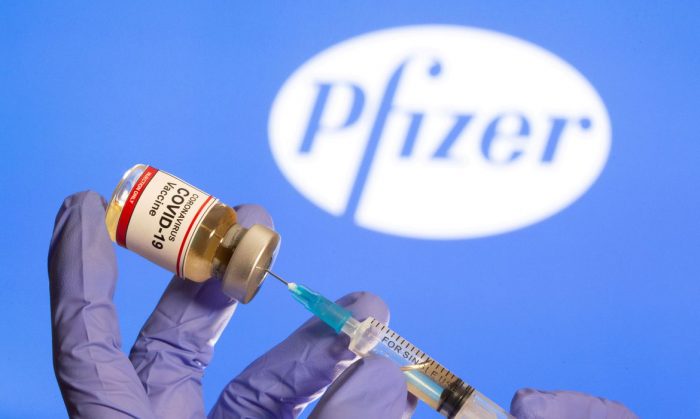
A Agência Nacional de Vigilância Sanitária (Anvisa) concedeu nesta terça-feira 23/2, o registro definitivo à vacina contra a covid-19 desenvolvida pela farmacêutica norte-americana Pfizer em parceria com a empresa de biotecnologia alemã BioNtech. A concessão do registro foi anunciada pelo diretor-presidente da agência reguladora, Antônio Barra Torres, que destacou que a análise para a liberação do imunizante levou 17 dias.
“O imunizante do Laboratório Pfizer/Biontech teve sua segurança, qualidade e eficácia aferidas e atestadas pela equipe técnica de servidores da Anvisa, que prossegue no seu trabalho de proteger a saúde do cidadão brasileiro”, disse Barra Torres ao anunciar o registro. “Esperamos que outras vacinas estejam, em breve, sendo avaliadas e aprovadas”, acrescentou.
A vacina é a primeira a obter o registro definitivo no Brasil. O imunizante se chama Cominarty. A empresa entrou no dia 6 de fevereiro com o pedido de registro definitivo da vacina contra a covid-19. O imunizante, entretanto, ainda não está disponível no país.
Em dezembro, a Pfizer já havia anunciado que não faria pedido para uso emergencial da sua vacina no Brasil, e que seguiria o processo de submissão diretamente para um registro definitivo. À época, a empresa disse considerar o procedimento “mais célere”, além de mais amplo.
Segundo a Pfizer, 2,9 mil voluntários participaram dos testes clínicos de sua vacina no Brasil. No mundo todo, foram 44 mil participantes em 150 centros de seis países, incluindo África do Sul, Alemanha, Argentina, Estados Unidos e Turquia. Os resultados da terceira e última fase de testes do imunizante, divulgados em novembro, apontaram eficácia de 95% contra o novo coronavírus (covid-19).
De acordo com a Anvisa, o registro “abre caminho para a introdução no mercado de uma vacina com todas as salvaguardas, controles e obrigações resultantes dessa concessão”. Até então, as vacinas aprovadas no Brasil são para uso emergencial: a CoronaVac, produzida pelo Instituto Butantan em parceria com a farmacêutica chinesa Sinovac, e a vacina produzida pela Fundação Oswaldo Cruz (Fiocruz) em parceria com a Universidade de Oxford e o laboratório inglês AstraZeneca.
De acordo com a Anvisa, entre as autoridades referendadas pela Organização Pan-Americana da Saúde (Opas), a agência reguladora brasileira é a primeira a conceder o registro de uma vacina contra a covid-19.
O pedido de registro definitivo é o segundo que a Anvisa recebe para uma vacina contra a covid-19. O primeiro foi feito em 29 de janeiro e é relativo à vacina desenvolvida pela farmacêutica AstraZeneca em parceria com a Universidade de Oxford, que já tem autorização para uso emergencial no país.
Fotografia/Fonte: Agência Brasil